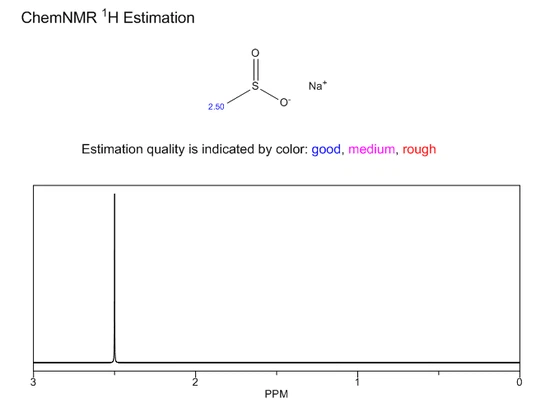
Metanosulfinato de sodioes un compuesto orgánico. Suele aparecer como un polvo o cristal de color blanco a blanco grisáceo sin olor especial. A altas temperaturas, el metanosulfito de sodio puede presentar una ligera sublimación. Cuando se calienta a aproximadamente 120 grados, el metanosulfito de sodio perderá su agua cristalina y se descompondrá gradualmente. Por ejemplo, tiene reducibilidad y puede reaccionar con peróxido de hidrógeno en soluciones acuosas ácidas o neutras para generar sulfito de peroximetano. El sulfito de peroximetano es muy inestable y se descompone rápidamente en iones de sulfato, agua y oxígeno. Además, el metanosulfonato de sodio también puede sufrir una reacción de oxidación-reducción con ácido hipocloroso, generando clorometano, iones sulfato y agua. Se ha descrito la adición conjugada de metanosulfonato de sodio con heterociclos vinílicos. Estudió la reacción de acoplamiento cruzado entre el ácido arilborónico y el metanosulfonato de sodio. Su solución de reserva se prepara añadiendo 1 equivalente de hidróxido de sodio al ácido metanosulfónico y diluyéndolo a 4M. Mantener el envase sellado, almacenar en recipiente cerrado, en lugar fresco y seco, evitar el contacto con óxidos y humedad, usar y almacenar según especificaciones sin descomposición.

|
|
|
|
Fórmula química |
CH3NaO2S |
|
Masa exacta |
102 |
|
Peso molecular |
102 |
|
m/z |
102 (100.0%), 104 (4.5%), 103 (1.1%) |
|
Análisis elemental |
C, 11,77; H, 2,96; Na, 22,52; O, 31,35; S, 31,41 |
metanosulfinato de sodio, es una sal inorgánica con un conjunto distinto de propiedades y aplicaciones. Aparece como un sólido cristalino de color blanco que es soluble en agua, formando una solución acuosa. Este compuesto se caracteriza por la presencia de un grupo sulfinato (SO2-), donde uno de los átomos de oxígeno del ion sulfato (SO42-) ha sido reemplazado por un átomo de hidrógeno, y este grupo está unido a un catión sodio (Na+).
En cuanto a su preparación, puede sintetizarse mediante diversas reacciones químicas, como la oxidación del metanotiol (CH3SH) con agentes oxidantes apropiados en condiciones controladas. El proceso requiere un manejo cuidadoso debido a la posible reactividad de los intermedios involucrados.
Este compuesto encuentra utilidad en varios entornos industriales y de investigación. Una de sus aplicaciones clave es como agente reductor en diversas reacciones químicas, particularmente en aquellas que requieren condiciones de reducción suaves y selectivas. Además, se emplea en la producción de otras sustancias químicas y sirve como intermediario en rutas sintéticas que conducen a una amplia gama de productos.
Además, su capacidad para formar radicales estables en condiciones específicas lo hace valioso en estudios que involucran química radical y radicales libres. Los investigadores utilizan sus propiedades únicas para investigar mecanismos de reacción, estudios cinéticos y otros aspectos de procesos mediados por radicales-.
En general, con su estructura química y propiedades distintivas, desempeña un papel importante tanto en los procesos industriales prácticos como en la investigación química avanzada.


Síntesis Orgánica
Puede utilizarse para sintetizar ciertos compuestos orgánicos específicos. Por ejemplo, puede reaccionar con aldehídos o cetonas para generar los correspondientes éteres de metilsulfonilalquilo, que son importantes intermedios de síntesis orgánica. Además, también se puede utilizar para sintetizar algunos compuestos biológicamente activos.
Como agente quelante y precipitante
Tiene la capacidad de formar quelatos estables con iones metálicos, lo que le permite extraer iones metálicos de soluciones acuosas. Los agentes quelantes mejoran la estabilidad y solubilidad de los iones metálicos formando una estructura de anillo con iones metálicos, facilitando así la separación y extracción de iones metálicos de sistemas acuosos complejos.
También se puede utilizar como precipitante para precipitar ciertos iones o compuestos específicos. La función del precipitante es reaccionar químicamente con iones o compuestos en la solución para producir un precipitado que es insoluble en agua, logrando así la separación y purificación de iones.


En el campo de la agricultura
Como por ejemplo ser utilizados como materia prima o aditivos para pesticidas, para prevenir enfermedades y plagas, o para promover el crecimiento de las plantas.
Ciencias Ambientales
Debido a su reducibilidad y otras propiedades químicas, el metanosulfito de sodio también tiene cierto valor de aplicación en el campo de las ciencias ambientales. Por ejemplo, puede utilizarse para abordar determinadas cuestiones de contaminación ambiental, o para estudiar los mecanismos de transformación y degradación de determinadas sustancias en el medio ambiente.

Caso de experimento de investigación
El objetivo principal de este experimento de investigación fue establecer un método para la determinación simultánea de iones cloruro (Cl-) y sulfato (SO42-) enmetanosulfinato de sodiomediante cromatografía iónica.
Materiales y métodos
Preparación de muestras
- Las muestras se prepararon con concentraciones conocidas de iones Cl- y SO42-.
- Las muestras se prepararon en condiciones controladas para garantizar la precisión y reproducibilidad.
Instrumentación
- Se utilizó un sistema de cromatografía iónica equipado con un detector de conductividad de supresión.
- El sistema se calibró utilizando soluciones estándar de iones Cl- y SO42-.
Condiciones cromatográficas
- Se optimizaron las condiciones cromatográficas apropiadas, como la composición de la fase móvil, el caudal y la temperatura de la columna, para garantizar la separación y detección de iones Cl- y SO42-.
Análisis de datos
- Se midieron las áreas de los picos de los iones Cl- y SO42- y se compararon con la curva de calibración para determinar sus concentraciones en las muestras.
- Se calcularon las tasas de recuperación y las desviaciones estándar relativas (RSD) para evaluar la exactitud y precisión del método.
Resultados
Curva de calibración
- La curva de calibración para Cl- fue lineal en el rango de 0,2 a 25 mg/l con un coeficiente de correlación (r) de 0,9999.
- La curva de calibración para SO42- fue lineal en el rango de 0,1~10 mg/L con una r de 0,9996.
Recuperación y Precisión
- La recuperación media de Cl- fue del 102 % con una RSD del 0,36 %.
- La recuperación media de SO42- fue del 101% con una RSD del 0,61%.
Límites de detección
- Los límites de detección de Cl- y SO42- fueron 0,011 mg/L y 0,014 mg/L, respectivamente.
El experimento de investigación estableció con éxito un método para la determinación simultánea de iones Cl- y SO42- enmetanosulfinato de sodiomediante cromatografía iónica. El método mostró un buen rango lineal, límites de detección bajos y alta exactitud y precisión. Los resultados obtenidos de este estudio son confiables y pueden usarse con fines de control de calidad en la producción y el análisis.
El método desarrollado tiene aplicaciones potenciales en diversas industrias donde se utiliza, como la farmacéutica, colorantes, polímeros y la industria alimentaria. Al determinar con precisión las concentraciones de iones Cl- y SO42- que contiene, los fabricantes pueden garantizar la calidad y consistencia de sus productos.
En conclusión, el experimento de investigación demostró la viabilidad de utilizar la cromatografía iónica para la determinación simultánea de iones Cl- y SO42-. El método desarrollado es confiable, exacto y preciso, y tiene aplicaciones potenciales en diversas industrias.

El metanosulfonato de sodio (número CAS 20277-69-4) es un importante intermedio de síntesis orgánica ampliamente utilizado en los campos de la medicina, pesticidas, colorantes y materiales funcionales. El método de síntesis central gira en torno a la introducción y conversión de grupos de ácido sulfónico, combinado con las necesidades de producción industrial y el progreso de la investigación de laboratorio, formando principalmente las siguientes tres rutas técnicas:
Método del metabisulfito de sodio: optimización de costes e innovación de procesos
El método del metabisulfito de sodio es actualmente el proceso principal en la producción industrial, que utiliza cloruro de metanosulfonilo y metabisulfito de sodio como materias primas para introducir de manera eficiente grupos de ácido sulfónico mediante una reacción de sustitución nucleofílica. El proceso específico es el siguiente:
En un matraz de cuatro bocas protegido con nitrógeno, agregue 326 gramos de solución de metabisulfito de sodio al 35% (fracción en masa), revuelva y caliente a 60-65 grados. El metabisulfito de sodio se descompone a esta temperatura para generar iones bisulfito, proporcionando sitios activos para reacciones posteriores.
Se añaden lentamente gota a gota 90,6 gramos de cloruro de metanosulfonilo y se mantiene un ligero reflujo de la solución de reacción. Durante el proceso de reacción, los iones bisulfito atacan el átomo de azufre del cloruro de metanosulfonilo, lo que lleva a una reacción de sustitución nucleofílica y la formación de sales de ácido sulfónico. Al utilizar una solución de hidróxido de sodio para ajustar el valor del pH en-tiempo real dentro del rango de 8-9, no solo previene la oxidación excesiva de los iones bisulfito a iones sulfato, sino que también evita la hidrólisis del cloruro de metanosulfonilo para producir ácido metanosulfónico.
Una vez completada la reacción, agregue una solución de cloruro de calcio al 50% (fracción de masa) para precipitar completamente el sulfito de calcio generado. Después de la filtración se obtiene una solución de sulfonación incolora y transparente que luego se concentra bajo deshidratación a presión reducida hasta que precipitan cristales blancos. Después de enfriar, se añadió etanol anhidro y se separó el cloruro de sodio por diferencia de solubilidad. Finalmente, se obtuvo metanosulfonato de sodio de alta-pureza mediante recristalización y secado.
Ventajas técnicas:
Rentabilidad:
El costo del metabisulfito de sodio es comparable al del sulfito de sodio, pero 1 mol de metabisulfito de sodio puede proporcionar 2 moles de iones de sulfito de hidrógeno, lo que aumenta la utilización de materia prima en un 50%;
Optimización de la solubilidad:
La solubilidad del metabisulfito de sodio es el doble que la del bisulfito de sodio, lo que reduce la cantidad de agua solvente y aumenta la capacidad de producción del equipo en más del 30%;
Simplificación de procesos:
Omitir los pasos de concentración y neutralización de múltiples-pasos en los métodos tradicionales para acortar el ciclo de producción.
Casos de aplicación:
Una determinada empresa química ha adoptado este proceso para lograr una producción anual de 500 toneladas de metanosulfonato de sodio, con una pureza del producto del 99,2% y una reducción integral de costos del 18% en comparación con los procesos tradicionales. Se utiliza ampliamente en la síntesis de zoxamida (un fármaco antiepiléptico) y Disperse Orange 29 (un tinte intermedio).
Método directo del sulfito de sodio: exploración para mejorar el proceso clásico.
El método directo del sulfito de sodio utiliza sulfito de sodio y cloruro de metanosulfonilo como materias primas para sintetizar metanosulfito de sodio a través de un mecanismo de sustitución nucleófila. El proceso es similar al método del metabisulfito de sodio, pero las condiciones de reacción deben optimizarse para superar el cuello de botella de la baja solubilidad del sulfito de sodio.
Utilizando un disolvente mixto de agua y etanol (relación de volumen 3:1), la solubilidad del sulfito de sodio se incrementó al 15 % (fracción de masa), que es tres veces mayor que la del sistema de agua pura. La temperatura de reacción se controla entre 70 y 75 grados para promover la frecuencia de colisión entre los iones sulfito y el cloruro de metanosulfonilo.
Divida el cloruro de metanosulfonilo en tres lotes y agréguelos gota a gota, con un intervalo de 15 minutos entre cada lote, para evitar reacciones secundarias causadas por una concentración local excesiva. El punto final de la reacción se controla mediante cromatografía de gases para garantizar una tasa de conversión mayor o igual al 98% para el cloruro de metanosulfonilo residual.
Presentamos la tecnología de cristalización asistida por ultrasonidos, aplicando ondas ultrasónicas de 20 kHz en la solución concentrada para hacer que la distribución del tamaño de las partículas de cristal sea más uniforme (D50=45 μ m) y reducir el tiempo de filtración en un 40 %.
Desafíos técnicos:
Costo de recuperación de solventes:
El etanol debe recuperarse mediante destilación, cuyo consumo de energía representa el 12% de los costos de producción;
Por control de producto:
El ácido metanosulfónico se genera fácilmente a altas temperaturas (rendimiento menor o igual al 2%), que debe suprimirse mediante la regulación del pH en tiempo real-.
Escenarios aplicables:
Adecuado para preparaciones de laboratorio-a pequeña escala o productos-de alta gama sensibles a impurezas (como metanosulfonato de sodio de grado farmacéutico, pureza mayor o igual al 99,5 %).
Método Redox: un camino emergente en la química verde
El método de oxidación-reducción regula el estado de valencia de los elementos de azufre mediante reacciones de oxidación o reducción, proporcionando una alternativa ecológica para la síntesis demetanosulfinato de sodio.
Utilizando metilmercaptano (CH3SH) como materia prima, reacciona con el oxígeno bajo la acción de un catalizador (como el óxido a base de vanadio) para producir metanosulfonato de sodio. Las condiciones de reacción son 120 grados y 2,5 MPa, con una selectividad del 92%. Las materias primas para esta ruta están fácilmente disponibles (el metilmercaptano es un subproducto de los petroquímicos), pero es necesario abordar la cuestión de la desactivación del catalizador (vida útil inferior o igual a 500 horas).
Se redujo selectivamente disulfuro de dimetilo ((CH3)2S2) para producir metanosulfonato de sodio a 80 grados y 1,5 MPa bajo la acción de hidrógeno y catalizador de paladio-carbono, con un rendimiento del 85%. Esta ruta tiene una alta tasa de utilización atómica (100%), pero existen riesgos de seguridad asociados con el transporte y almacenamiento de hidrógeno.
Perspectivas tecnológicas:
El método de oxidación-reducción se ajusta a los principios de la química verde (economía atómica mayor o igual al 90%), pero su aplicación industrial aún está limitada por el costo del catalizador (precio del catalizador a base de vanadio mayor o igual a 5000 yuanes/kg) y las duras condiciones de reacción. Con el desarrollo de nanocatalizadores y tecnología de reactores de flujo continuo, se espera que esta ruta alcance una producción a gran-escala antes de 2030.
Preguntas frecuentes
¿Para qué se utiliza el hidroximetanosulfinato de sodio?
+
-
Se utiliza hidroximetanosulfinato de sodio.como reactivo en la síntesis de compuestos orgánicos, como catalizador en reacciones químicas y como conservante y agente blanqueador.. El hidroximetanosulfinato de sodio también se utiliza en la producción de alimentos y bebidas, así como en la industria farmacéutica.
¿Cuál es la sal de sodio del ácido metanosulfónico?
+
-
Metanosulfonato de sodio| CH3NaO3S|CID 638112 - PubChem.
¿Es seguro el cumenosulfonato de sodio?
+
-
Se ha verificado que este químico es debaja preocupación en productos de limpiezabasado en datos experimentales y modelados evaluados por la EPA.
¿Cuál es otro nombre para el heptanosulfonato de sodio?
+
-
Sinónimos:Ácido 1-heptanosulfónicoSal de sodio. Sal sódica del ácido heptilsulfónico.
Etiqueta: metanosulfinato de sodio cas 20277-69-4, proveedores, fabricantes, fábrica, venta al por mayor, compra, precio, a granel, en venta