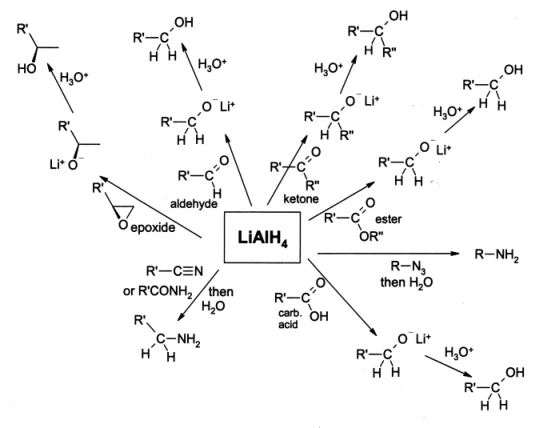
Hidruro de litio y aluminio(LAH) es un potente reactivo reductor elogiado por su amplia reactividad en las ciencias naturales. A pesar de sus limitaciones, convierte eficazmente ésteres, ácidos carboxílicos y aldehídos en alcoholes. Por ejemplo, el LAH es generalmente insuficiente en ciertas mezclas como alcanos y aromáticos, que necesitan grupos funcionales propensos a la descomposición. Además, los grupos potentes que atraen electrones impiden que el LAH reduzca los compuestos carbonílicos. Comprender estas limitaciones es fundamental para mejorar las reacciones y elegir los reactivos adecuados. En esta extensa guía, profundizaremos en estos imperativos e identificaremos sustancias que no se ven afectadas por el LAH, lo que ayudará a los físicos a tomar decisiones informadas en sus ensayos de ingeniería.
Comprensión del hidruro de litio y aluminio: una breve descripción general
Antes de profundizar en lo que no reacciona con el hidruro de litio y aluminio, repasemos brevemente qué es este compuesto y cómo se comporta normalmente en las reacciones químicas.
Hidruro de litio y aluminio, con la fórmula química LiAlH4, es un agente reductor potente que se utiliza habitualmente en la síntesis orgánica. Es especialmente eficaz para reducir compuestos carbonílicos, como aldehídos y cetonas, a alcoholes. El LAH también puede reducir ácidos carboxílicos, ésteres e incluso algunos enlaces triples carbono-nitrógeno.
La reactividad del LAH se debe a su capacidad para transferir iones hidruro (H-) a centros deficientes en electrones en moléculas orgánicas. Esta transferencia a menudo da como resultado la reducción de grupos funcionales, lo que convierte al LAH en un reactivo de referencia para muchos químicos orgánicos.
|
|
|
Grupos funcionales y compuestos resistentes a LAH
MientrasHidruro de litio y aluminio(LAH) es un potente especialista en reducción, no muestra una reactividad generalizada. El hecho de que algunos compuestos y grupos funcionales resistan las reacciones de LAH enfatiza la necesidad de una planificación cuidadosa en los productos sintéticos. Debido a los enlaces dobles y triples estables de los alquenos y alquinos, LAH generalmente no logra reducirlos. Además, los intensificadores como los grupos nitro y los peróxidos suelen ser inertes en condiciones de LAH. Comprender estas exenciones es fundamental para que los científicos realmente planifiquen cursos de ingeniería y descifren los resultados de las reacciones. Percibir cuándo funcionará o no LAH ayuda a elegir el reactivo adecuado para lograr los cambios de compuestos deseados.
A continuación se presentan algunos grupos funcionales y compuestos clave que normalmente no reaccionan con el hidruro de litio y aluminio:
Alcanos y alquenos
Los hidrocarburos saturados e insaturados sin grupos funcionales polares generalmente no reaccionan frente al LAH. La falta de centros deficientes en electrones en estas moléculas significa que no hay sitio para la transferencia de hidruros.
01
Compuestos aromáticos
La estabilidad de los anillos aromáticos los hace resistentes a la reducción por LAH. El benceno y sus derivados, por ejemplo, permanecen inalterados cuando se exponen a este agente reductor.
02
Éteres
Los éteres simples, como el éter dietílico o el tetrahidrofurano (THF), a menudo se utilizan como disolventes para reacciones de LAH porque no reaccionan con el compuesto.
03
Alcoholes
Si bien el LAH puede reducir aldehídos y cetonas a alcoholes, no reduce aún más los alcoholes a alcanos en condiciones normales.
04
Aminas
Las aminas primarias, secundarias y terciarias generalmente no reaccionan con el LAH. Sin embargo, cabe señalar que el LAH puede reducir ciertos óxidos de amina.
05
Factores que influyen en la reactividad de LAH y excepciones a la regla
Si bien la lista anterior proporciona una guía general, es importante tener en cuenta que la reactividad a veces puede depender de condiciones específicas o estructuras moleculares. Exploremos algunos factores que pueden influir en la reactividad de LAH y analicemos algunas excepciones a las reglas generales:
Impedimento estérico
En algunos casos, el impedimento estérico puede impedirHidruro de litio y aluminiode reaccionar con grupos que de otro modo serían reducibles. Por ejemplo, las cetonas o ésteres altamente impedidos podrían mostrar una reactividad reducida o incluso una resistencia total a la reducción de LAH.
Condiciones de reacción
El disolvente, la temperatura y el tiempo de reacción pueden influir en la reactividad del LAH. En algunos casos, cambiar estas condiciones puede permitir que el LAH reduzca grupos que normalmente no son reactivos. Por ejemplo, si bien los alcoholes generalmente no son reactivos, la exposición prolongada al LAH a temperaturas elevadas a veces puede provocar una mayor reducción.
Consideraciones estructurales
La estructura general de una molécula puede provocar a veces una reactividad inesperada. Por ejemplo, si bien los éteres simples no suelen ser reactivos, ciertos éteres cíclicos pueden experimentar reacciones de apertura de anillo con LAH en condiciones específicas.
Reacciones en competencia
En moléculas con múltiples grupos funcionales, la presencia de un grupo altamente reactivo puede dar lugar a resultados inesperados. Por ejemplo, si bien las aminas no suelen ser reactivas, una molécula que contenga tanto una amina como un grupo reducible (como una cetona) puede sufrir una reducción parcial o completa.
Comprender estos matices es fundamental para los químicos que trabajan con moléculas orgánicas complejas. Siempre es recomendable tener en cuenta toda la estructura molecular y las condiciones de reacción al predecir la reactividad de LAH.
Implicaciones prácticas y agentes reductores alternativos
Saber con qué no reaccionaHidruro de litio y aluminioes tan importante como comprender sus capacidades reductoras. Este conocimiento permite a los químicos:
- Diseñar rutas sintéticas más eficientes
- Proteger ciertos grupos funcionales durante las reacciones de reducción
- Elija disolventes apropiados para las reacciones LAH
- Predecir posibles reacciones secundarias o resultados inesperados
Cuando el LAH resulta ineficaz o inadecuado, los químicos tienen varios agentes reductores alternativos a su disposición. Algunas alternativas comunes incluyen:
Borohidruro de sodio (NaBH4)
Un agente reductor más suave que se utiliza a menudo para reducciones de carbonilo.
01
Hidruro de diisobutilaluminio (DIBAL-H)
Útil para reducciones selectivas de ésteres a aldehídos.
02
Gas hidrógeno con un catalizador metálico
Eficaz para reducir alquenos y alquinos.
03
Disolución de reducciones de metales (por ejemplo, reducción de Birch)
Útil para reducir compuestos aromáticos.
04
Cada una de estas alternativas tiene su propio conjunto de grupos funcionales reactivos y no reactivos, lo que permite a los químicos adaptar su elección de agente reductor a necesidades sintéticas específicas.
Conclusión
Hidruro de litio y aluminioes una herramienta poderosa en el arsenal del químico orgánico, pero no está exenta de limitaciones. Comprender qué no reacciona con LAH es crucial para una planificación sintética y un análisis de reacciones eficaces. Desde alcanos no reactivos y compuestos aromáticos hasta éteres y aminas típicamente resistentes, este conocimiento ayuda a los químicos a navegar por el complejo panorama de las reacciones orgánicas.
Recuerde que, si bien las reglas generales son útiles, pueden ocurrir excepciones en función de estructuras moleculares específicas, condiciones de reacción y funcionalidades en competencia. Siempre considere el contexto molecular completo al predecir la reactividad.
Ya sea que sea un estudiante que aprende química orgánica o un investigador experimentado que expande los límites de la síntesis, una comprensión profunda de las capacidades y limitaciones de LAH le será útil en sus esfuerzos químicos.
Referencias
Smith, MB y March, J. (2007). Química orgánica avanzada de March: reacciones, mecanismos y estructura. John Wiley & Sons.
Carey, FA y Sundberg, RJ (2007). Química orgánica avanzada: Parte B: Reacción y síntesis. Springer Science & Business Media.
Clayden, J., Greeves, N., y Warren, S. (2012). Química orgánica. Oxford University Press.
Kürti, L., y Czakó, B. (2005). Aplicaciones estratégicas de reacciones con nombre en síntesis orgánica. Elsevier.
Vollhardt, KPC y Schore, NE (2014). Química orgánica: estructura y función. WH Freeman and Company.